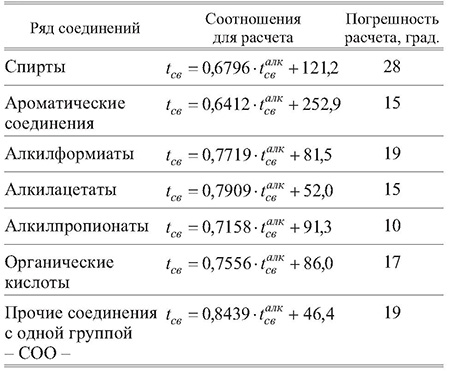
Уравнения для вычисления tcв методом сравнительного расчета приведены в табл. 7.
Пример. Рассчитать температуру самовоспламенения изоамилового эфира изомасляной кислоты по соотношениям табл. 7.
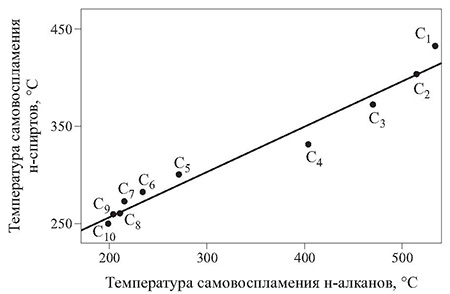
Рис.7. Взаимосвязь температур самовоспламенения алканов и спиртов
Структурная формула соединения имеет вид:
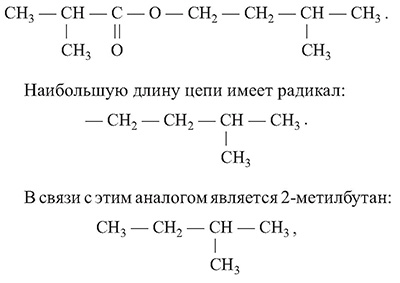
температура самовоспламенения которого равна 430°С.
Температура самовоспламенения изоамилового эфира изомасляной кислоты:
tсв = 0,8439 х 430 + 46,4 = 409°C.
Экспериментальное значение температуры самовоспламенения равно 390°С.
Таблица 7. Расчет температуры самовоспламенения сравнительным методом
Расчет концентрационных пределов распространения пламени жидкостей и газов
Нижний концентрационный предел распространения пламени индивидуальных веществ
Нижний концентрационный предел распространения пламени фн веществ, молекулы которых состоят из атомов C, H, О, N, S, Si, P, F и Cl, может быть вычислен по формуле:

Значения коэффициентов hj приведены в табл. 8.
Таблица 8. Значение коэффициентов hj формулы (20)
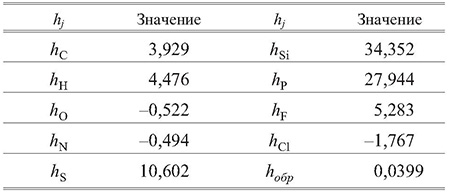
Относительная средняя квадратичная погрешность расчета по формуле (20) составляет 8%.
Пример. Рассчитать величину нижнего концентрационного предела распространения пламени хлорпропилтриэтоксисилана.
Исходные данные. Химическая формула хлорпропилтриэтоксисилана имеет вид C9H21O3ClSi. Стандартная теплота образования = -1212,51 кДж/моль.
Решение. C учетом приведенной формулы хлорпропилтриэтоксисилана имеем mC = 9; mH = 21; mO = 3; mCl =1; mSi = 1. Принимая значения коэффициентов hC, hH, hO, hCl и hSi по табл. 9, получаем
Фн = 100/(1 + 0,0399(-1212,51) + 3,929 • 9 + + 4,476 • 21 — 0,522 • 3 — 1,767 • 1 + + 34,352 • 1) = 0,88% об.
Экспериментальное значение нижнего концентрационного предела распространения пламени хлорпропилтриэтоксисилана равно 0,7% об.
Таблица 9. Значения коэффициентов и hj для различных классов химических соединений
| Класс соединений | hобр | hC | hH | hО | hC | hCl |
|---|---|---|---|---|---|---|
| Алканы | 0,0399 | 3,919 | 4,483 | — | — | — |
| Алифатические спирты | 0,0432 | 4,287 | 4,889 | -0,522 | — | — |
| Алкены | 0,0419 | 4,141 | 4,727 | — | — | — |
| Ароматические углеводороды | 0,0489 | 4,904 | 5,569 | — | — | — |
| Алкил-хлориды | 0,0399 | 3,919 | 4,483 | — | — | -0,586 |
| Алкиламины | 0,0360 | 3,501 | 4,006 | — | -0,494 | |
| Кетоны | 0,0453 | 4,534 | 5,142 | -0,522 |
|
|
| Альдегиды | 0,0490 | 4,936 | 5,583 | -0,522 |
|
|
| Карбоновые кислоты | 0,0594 | 6,087 | 6,847 | -0,522 |
|
|
| Эфиры карбоновых кислот | 0,0510 | 5,161 | 5,830 | -0,522 |
|
|
| Простые эфиры | 0,0415 | 4,113 | 4,679 | -0,522 |
|
|
Точность расчета по формуле (20) повышается при использовании коэффициентов и hj для отдельных классов химических соединений. Значения этих коэффициентов приведены в табл. 9.
Погрешность расчета Фн по формуле (20) с использованием коэффициентов табл. 9 составляет 5%.
Пример. Рассчитать величину нижнего концентрационного предела распространения пламени этилового эфира уксусной кислоты (этилацетата) по формуле (20).
Исходные данные. Химическая формула этил-ацетата имеет вид C4H8O2. Стандартная теплота образования = — 442,9 кДж/моль.
Решение. C учетом приведенной формулы этил-ацетата имеем mC =4; mH =8; mO = 2. Принимая значения коэффициентов hобр, hC, hH и hO по табл. 9, получаем
Фн = 100/(1 + 0,0510( -442,9) + 5,161 • 4 +5,830 • 8 — 0,522 • 2) = 2,2% об.
Экспериментальное значение нижнего концентрационного предела распространения пламени этилацетата равно 2,0% об.
Величину Фн можно вычислить по формуле:
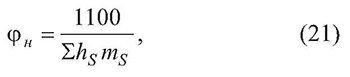
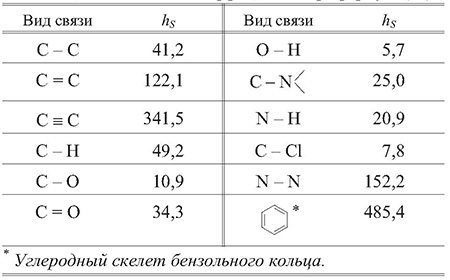
в которой hS — коэффициенты связей элементов, входящих в состав молекулы; mS — количество связей. Значения коэффициентов связей приведены в табл. 10.
Таблица 10. Значения коэффициентов hS в формуле (21)