Получение полной информации об изучаемом объекте складывается из следующих этапов:
1. Словесная гипотеза исследователя.
2. Логико-математическая модель биотехнологической системы микробиологического синтеза.
3. Системная схема процесса (структурно-функциональный портрет системы).
4. Вещественно-математическая модель.
5. Идентификация модели.
6. Проверка адекватности модели.
7. Использование модели для управления биотехнологическим процессом.
Построение логико-математической модели биотехнологических процессов производится в соответствии с некоторыми положениями теории относительно обособленных систем (ООС) (И. Н. Блохина, Г. А. Угодчиков, 1980). Под ООС понимается: на клеточном уровне — усредненная по ансамблю микробная клетка; на популяционном уровне — совокупность микробных клеток, усредненных по гомогенным частям популяции микроорганизмов одного вида; на биоценотическом уровне — совокупность усредненных микробных клеток по популяциям разных видов микроорганизмов.
На входы ООС любого уровня поступают экзогенные субстраты, а с выходов снимаются целевые продукты биосинтеза. ООС в каждом конкретном случае состоит из набора относительно обособленных подсистем (ООПС), имеющих два входа и один выход (рис. 3). На структурный вход А поступает поток вещества, из которого синтезируется продукт на выходе данной ООПС; на управляющий вход В поступает вещество, регулирующее синтез продукта на выходе С данной ООПС.
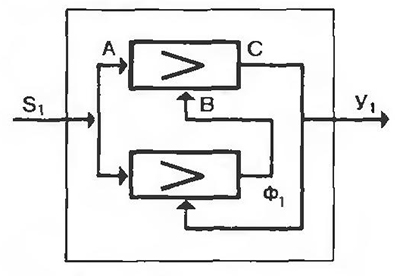
Рис. 3. Структурно-функциональный портрет системы для примера 1
Необходимо выделять лишь те ООПС, постоянные времени накопления продуктов на выходах которых одного порядка с постоянными времени накопления целевых продуктов. Именно они определяют биологическую инерцию и в дальнейшем называются ключевыми продуктами.
ООПС имеют три уровня иерархии:
1) ООПС, на управляющих выходах которых синтезируются ферменты;
2) ООПС, на управляющие выходы которых поступают вещества с выходов ООПС 1-го уровня;
3) ООПС, на управляющие выходы которых поступают вещества с выходов ООПС 2-го и 3-го уровней.
Концентрации ключевых продуктов на выходах описанных ООПС обозначим Ф1, К1, X1 соответственно. При определении функциональных связей между ООПС необходимо учитывать, что 1) на управляющий вход ООПС, на выходе которой образуется фермент, поступает поток вещества с ООПС, синтезом продукта которой управляет данный фермент; 2) на структурный вход ООПС, на выходе которой образуется фермент, поступает поток вещества, из которого образуется продукт ООПС, управляемой данным ферментом.
Приведенные положения удобно реализовать, применяя логико-математическую модель в виде прямоугольной матрицы. В общем случае, когда имеется несколько компонентов питательного субстрата и ферментов, катализирующих биологические реакции, она строится по следующим правилам:
1. Матрица разделена на две части вертикальным столбцом, которые образованы компонентами векторов X и Y, где X = (X1, Х2, …, Хn), Y = (Y1, Y2, …, Ym).
2. В первой строке левой части матрицы расположены компоненты векторов Ф, Y и X, которые соответствуют ключевым продуктам, управляющим синтезом продуктов ООПС-ами 2-го и 3-го уровней.
3. В первой строке правой части матрицы расположены компоненты вектора S, а также те компоненты векторов Ф, Y и X, которые соответствуют ключевым продуктам, поступающим на структурные входы ООПС 1-го, 2-го и 3-го уровней. В ячейках ставится «1» в левой части матрицы на пересечении строки и столбца, соответствующих рассматриваемому соединению и ключевому продукту, управляющему синтезом этого соединения. В правой части матрицы единица ставится на пересечении той же строки и столбца, соответствующего экзогенному субстрату или ключевому продукту, из которого образуется данное соединение. Остальные ячейки заполняются нулями.
Пример 1
Пусть биотехнологическая система микробиологического синтеза имеет один вход (рост на лимитирующем экзогенном субстрате, концентрация которого S1) и один выход. Целевой продукт — биомасса микробной популяции.
Допустим, исследователь считает, что динамика накопления биомассы определяется концентрацией фермента Ф1, управляющего наиболее медленной стадией в сложном комплексе биосинтетических процессов: целевой продукт (по мнению исследователя) образуется непосредственно из экзогенного субстрата, концентрация его Y1. Тогда логико-математическая модель в виде прямоугольной матрицы будет иметь следующий вид:
| Ф1 |
| S1 |
|---|---|---|
| 1 | Y1 | 1 |
Структурно-функциональный портрет системы (системная схема биотехнологического процесса) изображен на рис. 3.
Пример 2
Пусть по-прежнему биотехнологическая система микробиологического синтеза имеет один ход и один выход, но построена более сложная гипотеза, например, биологическая инерция процесса накопления биомассы определяется концентрацией рибосом, скорость синтеза которых, в свою очередь, ограничена концентрацией фермента Ф1, управляющего наиболее медленной стадией синтеза рибосом. Концентрация биомассы Х1, а концентрация рибосом Y1. Биомасса и рибосомы образуются непосредственно из экзогенного субстрата, концентрация которого S1. Тогда логико-математическая модель может быть представлена в виде
| Ф1 | Y |
| S1 |
|---|---|---|---|
| 0 | 1 | Х1 | 1 |
| 1 | 0 |
| 1 |
Структурно-функциональный портрет системы приведен на рис. 4.
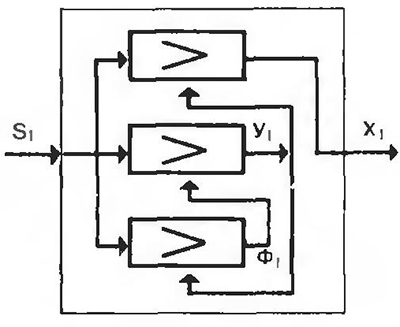
Рис. 4. Структурно-функциональный портрет системы для примера 2
Из приведенных примеров видно, что может быть создана такая система правил, согласно которой из логико-математических моделей однозначно выводятся структурно-функциональные портреты биотехнологических систем, а по ним строятся соответствующие вещественно — математические модели (И. Н. Блохина, В. И. Огарков, Г. А. Угодчиков, 1983).
В. В. Бирюков и В. М. Кантере (1985) рассматривают логико-математические и вещественно-математические модели биотехнологических процессов микробиологического синтеза различного типа:
- модели, основанные на описании функции отклика;
- булевы модели для интегральной оценки состояния;
- кинетические модели для решения задач оптимизации зависимостей режимных параметров от времени;
- макрокинетические модели для решения вопросов управления режимами аэрации и перемешивания, а также масштабирования.